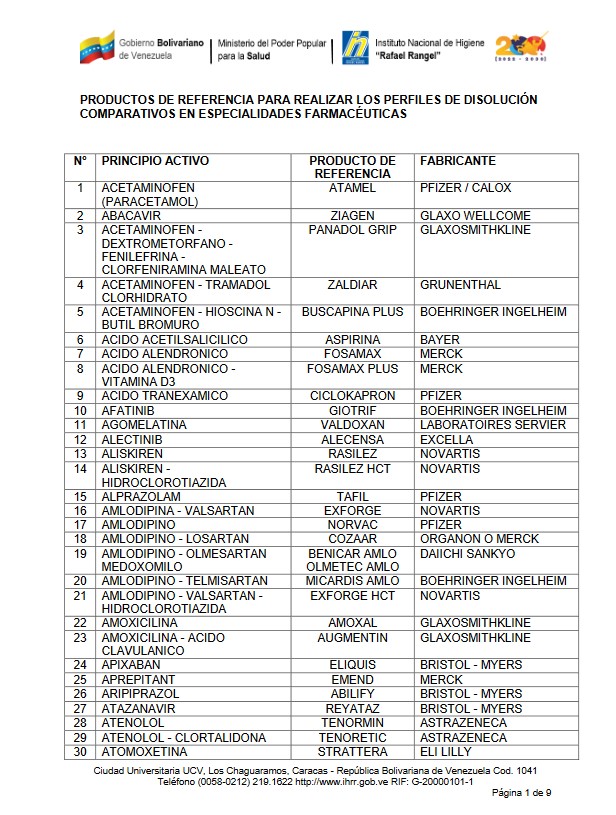
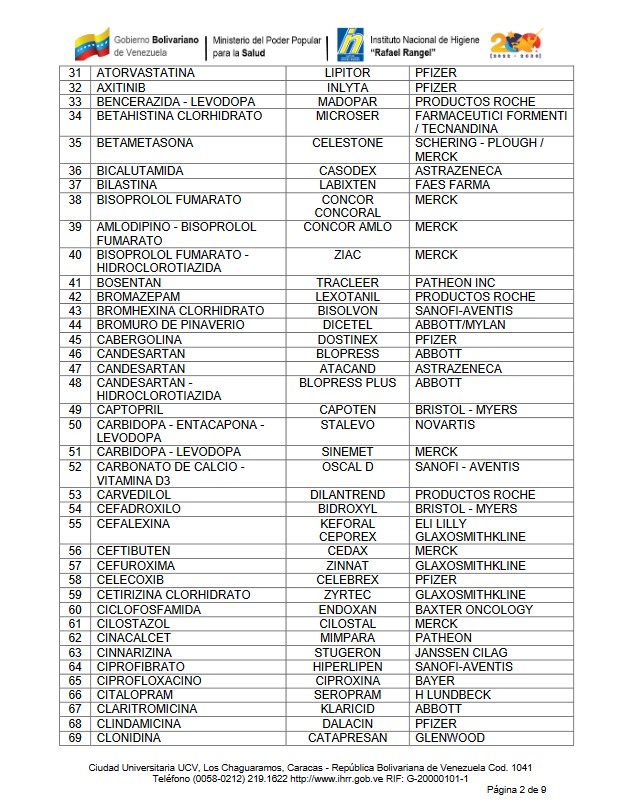
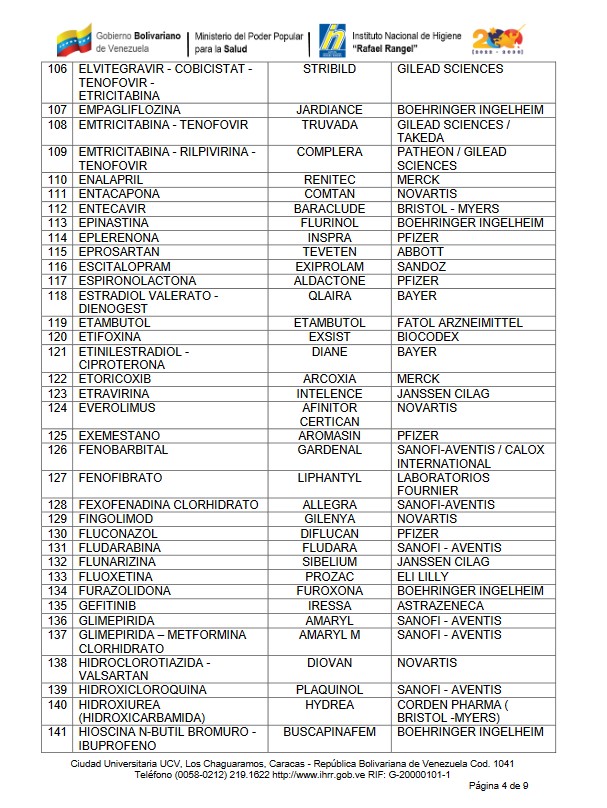
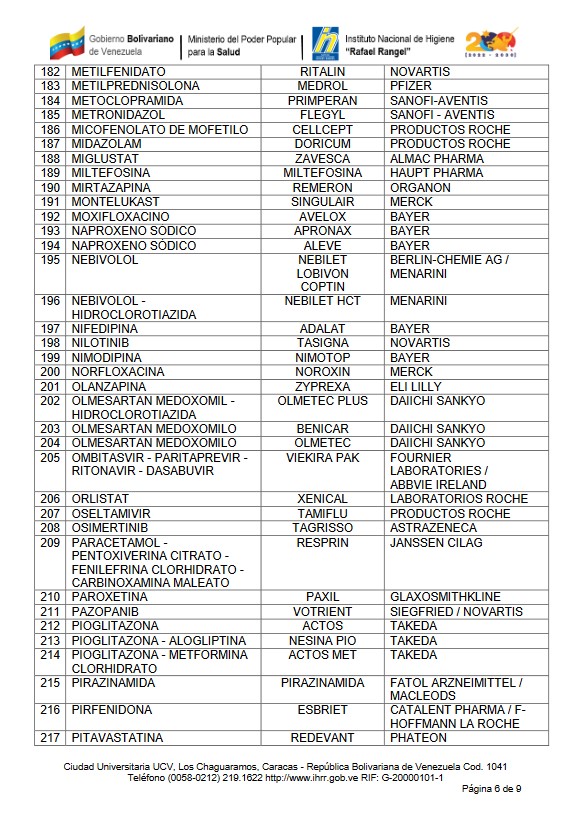
BIOEQUIVALENCIA
Se han identificado una serie de medicamentos cuya forma farmacéutica, liberación y vía de administración, hacen necesaria la demostración de la bioequivalencia, los cuales citan a continuación:
- Productos farmacéuticos de liberación inmediata para administración por vía oral que tengan una acción sistémica y para los cuales se cumplan uno o más de los criterios siguientes:
- Medicamentos de uso crítico.
- Medicamentos con rango terapéutico estrecho (márgenes de eficacia y seguridad) y curva dosis-respuesta de pendiente elevada.
- Existencia de evidencia documentada sobre problemas de biodisponibilidad o bioequivalencia relacionados con el principio activo o sus excipientes.
- Principios activos de la Clase III (“alta” solubilidad – “baja” permeabilidad) y Clase IV (“baja” solubilidad – “baja” permeabilidad).
- Evidencia científica que sugiera que los compuestos polimorfos del principio activo, los excipientes o los procesos de manufactura podrían afectar la bioequivalencia.
- Productos farmacéuticos que no sean administrados por la vía oral o por vía parenteral pero que estén destinados a actuar en forma sistémica
- Como los parches transdérmicos, los supositorios, los geles de testosterona y los implantes anticonceptivos).
- Productos farmacéuticos de liberación modificada destinados a actuar sistémicamente.
- Productos compuestos por una asociación a dosis fija con acción sistémica, que contenga un principio activo en el cual aplique la necesidad de realizar un estudio de bioequivalencia.
Los estudios de Biodisponibilidad y Bioequivalencia deben llevarse a cabo en centros o unidades, certificadas por el Instituto Nacional de Higiene “Rafael Rangel”, de acuerdo a lo dispuesto en las Normas Venezolanas de Biodisponibilidad y Bioequivalencia de Productos Farmacéuticos.
- Centros Especializados para Estudios de Biodisponibilidad y Bioequivalencia (CEEB): Que tengan dentro de su infraestructura todas las Unidades Especiales para Estudios de Biodisponibilidad y Bioequivalencia (UEEB). Su certificación tendrá una vigencia de (02) años.
- Unidades Especiales Contratadas para Estudios de Biodisponibilidad y Bioequivalencia (UECEB): Que son convenidas en forma individual por el Patrocinador del estudio. Estas Unidades pueden formar parte a su vez, de un Centro Especializado para Estudios de Biodisponibilidad y Bioequivalencia (CEEB). Su certificación tendrá una vigencia de un (01) año.
La solicitud la autorización de Centros o Unidades para realizar Estudios de Biodisponibilidad y Bioequivalencia, debe realizarse empleando los siguientes Formularios:
- F-PERC-045: Solicitud de Certificación de Centros Especializados para realizar Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-046: Solicitud de Certificación de Unidades Clínicas para realizar Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-047: Solicitud de Certificación de Unidades Bioanalitica donde realizan Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-048: Solicitud de Certificación de Unidades Estadísticas donde realizan Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-049: Solicitud de Certificación de Laboratorios de Análisis Clínicos que prestan servicios a los Centros Especializados o Unidades Clínicas donde se realizan Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-050: Solicitud de Renovación de Centros Especializados donde se realizan Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-051: Solicitud de Renovación de Unidades Clínicas donde realizan Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-052: Solicitud de Renovación de Unidades Bioanalitica donde realizan Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-053: Solicitud de Renovación de Unidades Estadísticas donde realizan Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-054: Solicitud de Renovación de Laboratorios de Análisis Clínicos que prestan servicios a los Centros Especializados o Unidades Clínicas donde se realizan Estudios de Biodisponibilidad/bioequivalencia.


En caso de requerir comunicarse o tener una audiencia con la Gerencia Sectorial de Registro y Control, deberá enviar correo electrónico a bioequivalencia.dasm.inhrr@


