Instructivos y Formularios
- Guia de Trámites, Consultas y Retroalimentación
- Guia Registro Usuario Empresa 2023»
- Guía para el Registro de Patrocinante 2023 »
- Guía Práctica para Digitalizar Archivo y Convertir en PDF »
- Guía Práctica para Crear y Reducir el tamaño de un PDF
- Guía Práctica para Comprimir Imágenes »
- Creación de Trámites Guía del Patrocinante-Tramitante Nov2015. »
- Seguimiento de Trámites Guía del Ftco. Patrocinante Nov2015 »
- Manual de e-Reporting para la Industria
- Guía de Farmacovigilancia para la Industria Farmacéutica
- Guía Para la Elaboración y Presentación de los Estudios de Estabilidad de Especialidades Farmacéuticas
- Guia de Trámites, Consultas y Retroalimentación
Especialidades Farmacéuticas y Productos Biológicos
REGISTRO SANITARIO
- Proceso para el Registro Sanitario de Productos farmacéuticos
- Instructivo para la consignación de la muestra»
- Instructivo para la consignación de expediente en físico »
- Instructivo para la consignación de la documentación electrónica clínica, preclínica o BE »
- Instructivo para elaborar las solicitudes de registro-SIVERC »
- Constancia de recepción »
- Preguntas Frecuentes SIVERC
- Instructivo para la consignación de las muestras solicitadas en el proceso de Registro Sanitario de Especialidades Farmacéuticas cuyo producto innovador no se encuentra Registrado en Venezuela.
- Instructivo para la consignación del expediente en físico para el Registro Sanitario de Especialidades Farmacéuticas cuyo producto innovador no se encuentra registrado en Venezuela.
- Instructivo para la consignación de la documentación electrónica solicitada en el proceso de Registro Sanitario de Especialidades Farmacéuticas cuyo producto innovador no se encuentra Registrado en Venezuela.
REGISTRO SANITARIO
- Instructivo para el Registro Sanitario de Productos Hemoderivados Homologos y Heterologos Categoría A1 Nov2015 »
- Instructivo para el Registro Sanitario de Productos Hemoderivados Homologos y Heterologos Categoría A2 Nov2015 »
- Instructivo para el Registro Sanitario de Productos Afines Homologos y Heterologos Categoría A1 Nov2015 »
- Instructivo para el Registro Sanitario de Productos Afines Homologos y Heterologos Categoría A2 Nov2015 »
- Instructivo para el Registro Sanitario de Productos Hemoderivados y Afines Categoría B1 Nov2015 »
- Instructivo para el Registro Sanitario de Productos Hemoderivados y Afines Categoría B2 Nov2015 »
- Instructivo para el Registro Sanitario de Productos Hemoderivados y Afines Categoría C Nov2015 »
- Instructivo de Muestra para el Registro Sanitario de Productos Hemoderivados y Afines, Homologos y Heterologos Nov2015 »
- Instructivo para el Registro Sanitario de Productos ADN Recombinantes, Anticuerpos Monoclonales y Terapéeuticos Categoría A1 Nov2015 »
- Instructivo para el Registro Sanitario de Productos ADN Recombinantes, Anticuerpos Monoclonales y Terapéeuticos Categoría A2 Nov2015 »
- Instructivo para el Registro Sanitario de Productos ADN Recombinantes, Anticuerpos Monoclonales y Terapéeuticos Categoría B1 Nov2015 »
- Instructivo para el Registro Sanitario de Productos ADN Recombinantes, Anticuerpos Monoclonales y Terapéeuticos Categoría B2 Nov2015 »
- Instructivo para el Registro Sanitario de Productos ADN Recombinantes, Anticuerpos Monoclonales y Terapéeuticos Categoría C Nov2015 »
- Instructivo de Muestra para el Registro Sanitario de Productos ADN Recombinantes, Anticuerpos Monoclonales y Terapéeuticos Nov2015 »
- Instructivo para el Registro Sanitario de Vacunas Categoría A1 Nov2015 »
- Instructivo para el Registro Sanitario de Vacunas Categoría A2 Nov2015 »
- Instructivo para el Registro Sanitario de Vacunas Categoría B1 Nov2015 »
- Instructivo para el Registro Sanitario de Vacunas Categoría B2 Nov2015 »
- Instructivo para el Registro Sanitario de Vacunas Categoría C Nov2015 »
- Instructivo de Muestra para el Registro Sanitario de Vacunas Nov2015 »
Para descargar un Formulario u Instructivo determinado debe hacer clic sobre el icono.
Solicitud para el Registro Nacional de Productos FarmaceuticosF-RCDM-023

Formularios – Productos Biológicos
Para descargar un Formulario u Instructivo determinado debe hacer clic sobre el icono. Modificación de Aspectos Legales durante el Registro Sanitario »
Modificación de Aspectos Legales durante el Registro Sanitario »
Para descargar un Formulario u Instructivo determinado debe hacer clic sobre el icono.
Debe leer detenidamente cada Instructivo de cada uno de los Formularios que se presentan a continuación para que su evaluación sea exitosa.
Toda modificación efectuada al producto o a las condiciones de comercialización establecidas en el registro sanitario del mismo, deben ser notificadas y autorizadas.
Debe emplear el o los formularios respectivos dependiendo del tipo de modificación a realizar y la clasificación de dicho cambio (IA, IB y II), en función de su impacto sobre la calidad, seguridad y eficacia del producto.
Para las modificaciones Postregistro de Aspectos Farmacéuticos, si su cambio no está abarcado en ninguno de los formularios F-PERC-060 al 066, debe emplear el formulario F-RCPB-038. Recuerde que en caso de dudas puede hacer sus consultas a través del correo divcnpb@gmail.com / divcnpb@inhrr.gob.ve
Para descargar un Formulario u Instructivo determinado debe hacer clic sobre el icono de descarga. La implementación de cambios en el producto registrado, sin la debida autorización conllevara a la cancelación del registro sanitario correspondiente.
Para descargar un Formulario u Instructivo determinado debe hacer clic sobre el icono.
Debe leer detenidamente cada Instructivo de cada uno de los Formularios que se presentan a continuación para que su evaluación sea exitosa.
La vigencia del registro sanitario de productos biológicos es de cinco (5) años, según lo establecido en la NORMA DE REGISTRO, LIBERACIÓN DE LOTE Y CONTROL DE LOS PRODUCTOS BIOLÓGICOS Nº N-PERC-001 de fecha 09/12/2008. »
Al menos 6 meses antes del vencimiento del registro sanitario, el representante del producto biológico a través del Farmacéutico Patrocinante, deberá solicitar la renovación del Registro Sanitario, empleando el formulario F-DMEF-005 Formulario de Solicitud de Renovación de Registro Sanitario
» según se indica en el Instructivo » respectivo, anexando los recaudos requeridos y cancelar la tarifa respectiva.
La solicitud de renovación del registro sanitario será improcedente en casos de pérdida de la vigencia terapéutica, incumplimiento de las condiciones de comercialización o problemas de calidad, seguridad o eficacia del producto.
Manual de Buenas Practicas de Evaluación para la Renovación de Registro Sanitario
Para descargar un Formulario u Instructivo determinado debe hacer clic sobre el icono.
Debe leer detenidamente cada Instructivo de cada uno de los Formularios que se presentan a continuación para que su evaluación sea exitosa.
| Título | Código | Formulario | Instructivo |
|---|---|---|---|
| Solicitud de Autorización de Protocolos Clínicos para Especialidades Farmacéuticas | F-RCDM-011 | ||
| Reporte de Eventos Adversos Serios Nacionales en Estudios Clínicosde Especialidades Farmacéuticas | F-RCDM-014 |
Para solicitar la autorización de un protocolo clínico de un producto biológico, deberán completar el formulario F-RCPB-064 Solicitud para Autorización de Protocolos Clínicos para Productos Biológicos » según lo indicado en el Instructivo » respectivo (VINCULO PARA AMBOS), remitir los recaudos requeridos y cancelar la tarifa correspondiente.
Una vez admitida la solicitud, será evaluada por la Unidad competente y en caso de conformidad, será autorizado por la Junta Revisora de Productos Farmacéuticos, según lo establecido en la Ley de Medicamentos.
Los protocolos clínicos autorizados, seran sometidos a inspección, momento en el cual el representante del producto deberá cancelar la tarifa establecida en la Gaceta Oficial de la República Bolivariana de Venezuela N° 39.819 del 13/12/2011.
Productos de Uso y Consumo Humano
La Dirección de Laboratorio Nacional de Control de Productos Alimentarios y Licores, como laboratorio de referencia del Ministerio del Poder Popular para la Salud, apoya con su conocimiento técnico-científico las políticas emanadas en materia de salud pública, realizando la evaluación integral de los productos de alimenticios consumidos por la población y ofreciendo respuesta a los programas de vigilancia sanitaria en materia alimenticia coordinados por el Servicio Autónomo de Contraloría Sanitaria.
Tiene entre sus funciones:
- Evaluación integral de Productos Alimentarios con fines de Registro Sanitario.
- Evaluación de Control de Calidad de Productos Alimentarios con fines de Control Sanitario.
- Evaluación de Desvíos de Calidad de Productos Alimentarios procedentes de Organismos del estado (Denuncias).
- Evaluación por Infección ó por intoxicación alimentaria (ETA).
- Ensayos Especiales con fines de control de calidad para productos alimentarios en general, servicios de recarga de agua potable, alimentos para animales, otros. (No conducente a Registro Sanitario)
- Ensayos Especiales con fines de elaboración del Etiquetado nutricional.
- Evaluación integral de Productos Alimentarios con fines de exportación de alimentos. (Certificados de Exportación)
- Alimento: No solamente las sustancia destinada a la nutrición del organismo humano, sino también, las que forman parte o se unen en su preparación, composición y conservación; las bebidas de todas clases y aquellas otras sustancias, con excepción de los medicamentos, destinados a ser ingeridos por el hombre. (Reglamento General de Alimentos. Gaceta Oficial de Venezuela Nº 25.864 del 16 de Enero de 1959).
- Calidad: Abarca los atributos que hacen referencia a la presentación, composición, pureza, tratamiento tecnológico y conservación que influyen en el valor de un producto para el consumidor.
- Evaluación Integral es la valoración de los Alimentos para verificar los requisitos de Calidad e Inocuidad establecidos en la normativa legal vigente, con el fin de determinar si son aptos para el consumo humano. Esta evaluación comprende: la revisión de la documentación, Ensayos Microbiológicos, Fisicoquímicos y Contaminantes.
- Fórmula cuali- cuantitativa: Consiste en la descripción de los componentes que integran un producto alimenticio, y la proporción en la que se encuentran en el producto expresada tanto en la unidad del sistema métrico correspondiente (g ; Kg; L; ml), y en el equivalente a su participación dentro de la fórmula del producto en porcentaje (%)
- Inocuidad: Condición de los alimentos que garantiza que no causarán daño al consumidor cuando se preparen y/o consuman de acuerdo con el uso al que se destinan. FAO/OPS.
- Recaudos: Se refiere a toda la información necesaria para conformar el expediente del Producto Alimenticio a ser evaluado. Consiste en detalles técnicos específicos que resultan necesarios para efectuar el ensayo en el laboratorio. Entre ellos se encuentran: Solicitud de Ensayo al laboratorio con fines de Registro Sanitario, Petición de Examen o Petición de Análisis, Comunicaciones para Ensayos especiales, Diagrama de flujo del proceso de fabricación, Formula cualitativa-cuantitativa, Rótulo y otra información pertinente.
- Solicitante/ Tramitante: Persona autorizada para realizar los tramites correspondientes a solicitudes de ensayo con fines de Registro, Control Sanitario y/o Ensayos Especiales. Para realizar los ensayos con fines de Registro Sanitario la persona debe presentar la documentación que lo acredite para realizar dicho trámite.
¿QUÉ SON LAS ENFERMEDADES TRANSMITIDAS POR ALIMENTOS (ETA)?
“Síndrome originado por la ingestión de alimentos y/o agua, que contengan agentes etiológicos en cantidades tales que afecten la salud del consumidor a nivel individual o grupos de población.”
“LAS ALERGIAS POR HIPERSENSIBILIDAD INDIVIDUAL A CIERTOS ALIMENTOS NO SE CONSIDERAN ETA”. Fuente: http://www.mpps.gob.ve
¿CUÁL ES LA CLASIFICACIÓN DE LAS ETA?
Infección Alimentaria: Resultan de la ingestión de alimentos que contienen la presencia de bacterias u otros microorganismos vivos (como virus, parásitos, hongos) los cuales infectan el cuerpo después del consumo.
Intoxicación Alimentaria: Refiere a la ingestión de toxinas que se encuentran en:
- Tejidos de plantas o animales,
- Productos metabólicos de microorganismos en los alimentos,
- Sustancias químicas que se incorporan de modo accidental, incidental o intencional en los alimentos.
Ocurren cuando las toxinas o venenos (de bacterias o mohos) están presentes en el alimento, incluyendo exotoxinas producidas por el metabolismo de las bacterias. Estas toxinas pueden estar presentes incluso cuando el microorganismo que las produjo ha sido eliminado o esté incapacitado para provocar infección. Fuente: http://www.panalimentos.org
¿QUIÉNES PODEMOS SUFRIR UNA ETA?
Todos somos susceptibles a contraer una enfermedad transmitida por los alimentos. Algunos grupos demográficos están a mayor riesgo que otros como son:
- Los lactantes y niños pequeños debido a que su sistema inmunológico no está completamente desarrollado como el de los adultos.
- Los ancianos, debido a que la efectividad de su sistema inmunológico ha disminuido con la edad.
- Individuos enfermos cuyos sistemas inmunológicos no están funcionando apropiadamente por causa de padecimientos como el cáncer, sida u otras enfermedades.
- Mujeres embarazadas y sus fetos.
¿CÓMO RECONOCER QUE ESTAMOS EN PRESENCIA DE UNA ETA?
Se pueden evidenciar varios síntomas como: malestar estomacal, diarrea, náusea, vómito, fiebre, escalofríos, dolores abdominales, dolor de cabeza, mareos u otros; si esto ocurre a las pocas horas de haber ingerido alimentos, y además le ocurre a otra persona (que haya ingerido los mismos alimentos), podemos entonces sospechar que estamos en presencia de una ETA. Lo más recomendable es buscar asistencia en un Centro de Salud (Ambulatorio, Hospital o Servicio de Salud Privado).
¿CUÁL ES EL PROCEDIMIENTO A SEGUIR ANTE UN BROTE DE ETA?
Una vez que se recibe asistencia médica (nivel de asistencia primaria), el médico debe determinar si está en presencia de una ETA, y conjuntamente con el epidemiólogo debe proceder a realizar la denuncia en el Distrito Sanitario al cual pertenece el Centro de Salud; para así iniciar la investigación epidemiológica.
El nivel de atención primaria (Centro de Salud) debe disponer de modelos de encuesta epidemiológica y materiales para toma de muestras; a fin de que el personal, tan pronto detecte los primeros casos, pueda recolectar la información preliminar y proceder a la toma de muestras clínicas hasta que llegue el personal del Distrito Sanitario correspondiente o equipo de investigación a completar el estudio.
Ésta investigación incluye una revisión de la información de casos de ETA que hayan llegado al servicio de salud, para detectar las similitudes en relación a la fecha de inicio de los síntomas, número de enfermos, síntomas predominantes, alimentos sospechosos, lugar y hora cuando se consumió el alimento sospechoso (aquellos consumidos dentro de las 72 horas anteriores al inicio de los síntomas) y cualquier otra información de interés epidemiológico.
El personal del Distrito Sanitario correspondiente o equipo de investigación se desplazará a la mayor brevedad posible hacia los sitios donde se encuentran los comensales expuestos, (enfermos o no) y al local donde se preparó o consumió la comida sospechosa. La rapidez tiene como objetivo efectuar oportunamente las encuestas, la recolección de las muestras de alimentos sospechosos, muestras ambientales y muestras biológicas de las personas afectadas, antes que los pacientes reciban antibióticos y los alimentos sean eliminados.
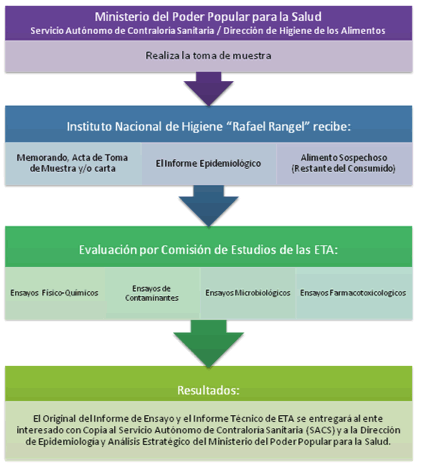
PASOS A SEGUIR PARA LA NOTIFICACIÓN DE UN BROTE DE ETA
EVALUACIÓN CON FINES DE REGISTRO SANITARIO
| N° | Recaudo a consignar | Instrucción |
|---|---|---|
| 1 | FORMULARIO F-DARM-001(*) | Descargue el Formulario Siga indicaciones del Instructivo de llenado Asegúrese de haber completado los campos con la información correcta de la muestra que va a someter a evaluación integral con fines de registro. Imprima 2 ejemplares Firme el Formulario Coloque un timbre fiscal equivalente a 0,02 U.T o en su defecto cancelar BANCO DE VENEZUELA 0102-0552-2100-0002-4439 o BANCO DEL TESORO 0163-0903-6290-3200-0282 o BANCO BICENTENARIO 0175-0378-2600-7171-7576 el Timbre Fiscal a nombre del Gobierno Distrito Capital G-200002123 NO SE ACEPTARÁN FORMULARIOS LLENADOS A MANO. |
| 2 | Registro de Información Fiscal (RIF) | Copia |
| 3 | Fórmula Cuali- Cuantitativa del producto a evaluar (ver definiciones) (*) | En 100g o en 100mL |
| 4 | Diagrama de flujo del proceso de fabricación (*) | Describa el proceso de fabricación, indicando las condiciones de tiempo y temperaturas aplicadas. |
| 5 | Modelo de Rótulo o Etiqueta del Producto (*) | Consignar Un (1) Rótulo o Etiqueta del Producto Este modelo deberá contener como mínimo la información de Nombre, Marca, Lote, Fecha de elaboración y Fecha de Vencimiento |
| 6 | Acta de toma de muestra del SENIAT. (para Bebidas alcohólicas nacionales) | Consignar copia |
| 7 | Resultado No Conforme | Copia del resultado analítico con resultado No Conforme. |
| 8 | Muestra Representativa. | Consultar L-DARM-001 Cantidad Mínima de Productos Alimenticios requeridas para el ensayo |
| 9 | Transferencia bancaria con el importe correspondiente al análisis solicitado (ver Regimen tarifario) | Cuenta para transferencia: Banco de Venezuela a la cuenta número N° 0102-0132-2900-0002-3650 RIF G-20000101-1 Consignar una (1) copia |
| 10 | Comprobante de citas | Consignar una (1) copia |
| 11 | Formato identificación del sobre | Imprimir y colocar en el sobre donde entregará toda la documentación |
| (*) EXCEPTO CERTIFICADO DE ANALISIS DE EXPORTACIÓN Coloque esta documentación en un sobre manila debidamente identificado en su parte frontal con el recaudo “Formato de identificación del sobre” Una vez asignada su cita, digitalice los recaudos indicados en formato PDF. (Máximo 300 MB) y envíe vía correo electrónico a la siguiente dirección: divcalimentos@gmail.com | ||
EVALUACIÓN CON FINES DE CONTROL SANITARIO
Verificación periódica de la calidad e inocuidad de los alimentos enmarcada dentro de los planes de Vigilancia Sanitaria del Servicio Autónomo de Contraloría Sanitaria
| N° | Recaudo a consignar | Instrucción |
|---|---|---|
| 1 | ACTA DE TOMA DE MUESTRAS EMITIDA POR FUNCIONARIO DE SACS QUE EFECTUA EL PROCEDIMIENTO | Consignar en físico Asegurarse que se encuentren los datos de la persona responsable por la empresa |
| 2 | Muestra Representativa. | Procedente de la Toma efectuada por el funcionario que ejecuta el procedimiento |
ENSAYOS ESPECIALES
EVALUACIÓN DE SERVICIOS DE RECARGA DE AGUA POTABLE, CONTROL DE CALIDAD PARA EMPRESAS, ENSAYOS DE INVESTIGACIÓN, OTRA SOLICITUD QUE NO CALIFIQUE EN LOS ÍTEMS ARRIBA MENCIONADOS (NO CONDUCENTE A REGISTRO SANITARIO)
| N° | Recaudo a consignar | Instrucción |
|---|---|---|
| 1 | FORMULARIO SOLICITUD DE REQUERIMIENTO * | Descargue el Formulario Complete la información según sea el caso de su solicitud Imprima 2 ejemplares y consigne el día de su cita |
| 2 | Transferencia bancaria con el importe correspondiente al análisis solicitado (ver Regimen tarifario) | Cuenta para transferencia: Banco de Venezuela a la cuenta número N° 0102-0132-2900-0002-3650 RIF G-20000101-1 Consignar una (1) Copia |
| 3 | Muestra Representativa. | Consultar L-DARM-001 Cantidad Mínima de Productos Alimenticios requeridas para el ensayo |
| 4 | Comprobante de citas | Solicite su Cita a través de nuestra Oficina Virtual Consignar una (1) copia |
| 5 | Formato identificación del sobre | Imprimir y colocar en el sobre donde entregará toda la documentación |
Coloque esta documentación en un sobre manila debidamente identificado en su parte frontal con el recaudo “Formato de identificación del sobre” Una vez asignada su cita, digitalice los recaudos indicados en formato PDF. (Máximo 300 MB) y envíe vía correo electrónico a la siguiente dirección: divcalimentos@gmail.com | ||
EVALUACIÓN POR ENFERMEDADES TRANSMITIDAS POR ALIMENTOS (ETA`s) / DESVIOS DE CALIDAD PROCEDENTES DE ORGANISMOS DEL ESTADO/ EVALUACIÓN DE CALIDAD SANITARIA DE COMEDORES (OFICIAL)
| N° | Recaudo a consignar | Instrucción |
|---|---|---|
| 1 | Acta de toma de muestra ó Comunicación dirigida a Presidencia del Instituto Nacional de Higiene “Rafael Rangel” (según aplique) | Consignar en físico |
| 2 | INFORME EPIDEMIOLOGICO (ETA`s) | Asegurarse que se encuentren los datos de la persona responsable de la emisión del informe (nombre, numero de contacto) |
| 3 | Muestras objeto del estudio |
ETIQUETADO NUTRICIONAL
| N° | Recaudo a consignar | Instrucción |
|---|---|---|
| 1 | FORMULARIO SOLICITUD DE REQUERIMIENTO * | Descargue el Formulario Complete la información según sea el caso de su solicitud Imprima 2 ejemplares y consigne el día de su cita |
| 2 | Muestra Representativa. | Consigne un (1) empaque del producto a evaluar |
| 3 | Transferencia bancaria con el importe correspondiente al análisis solicitado (ver Regimen tarifario) | Cuenta para transferencia: Banco de Venezuela a la cuenta número N° 0102-0132-2900-0002-3650 RIF G-20000101-1 Consigna una (1) Copia |
| 4 | Comprobante de citas | Solicite su Cita a través de nuestra Oficina Virtual Consignar una (1) copia Si está solicitando Ensayo para Registro Sanitario, solo consigne un (1) comprobante para ambas solicitudes |
| 5 | Formato identificación del sobre | Imprimir y colocar en el sobre donde entregará toda la documentación Si está solicitando Ensayo para Registro Sanitario, solo consigne un (1) sobre identificado para ambas solicitudes |
Coloque esta documentación en un sobre manila debidamente identificado en su parte frontal con el recaudo “Formato de identificación del sobre” Una vez asignada su cita, digitalice los recaudos indicados en formato PDF. (Máximo 300 MB) y envíe vía correo electrónico a la siguiente dirección: divcalimentos@gmail.com | ||
CERTIFICADOS DE ANÁLISIS PARA EXPORTACIÓN DE ALIMENTOS
| N° | Recaudo a consignar | Instrucción |
|---|---|---|
| 1 | FORMULARIO F-DARM-001(*) | Descargue el Formulario Siga indicaciones del Instructivo de llenado Asegúrese de haber completado los campos con la información correcta de la muestra que va a someter a evaluación integral con fines de registro. Imprima 2 ejemplares Firme el Formulario Coloque un timbre fiscal equivalente a 0,02 U.T o en su defecto cancelar BANCO DE VENEZUELA 0102-0552-2100-0002-4439 o BANCO DEL TESORO 0163-0903-6290-3200-0282 o BANCO BICENTENARIO 0175-0378-2600-7171-7576 el Timbre Fiscal a nombre del Gobierno Distrito Capital G-200002123 NO SE ACEPTARÁN FORMULARIOS LLENADOS A MANO. |
| 2 | Registro de Información Fiscal (RIF) | Copia |
| 3 | Fórmula Cuali- Cuantitativa del producto a evaluar (ver definiciones) (*) | En 100g o en 100mL |
| 4 | Diagrama de flujo del proceso de fabricación (*) | Describa el proceso de fabricación, indicando las condiciones de tiempo y temperaturas aplicadas. |
| 5 | Modelo de Rótulo o Etiqueta del Producto (*) | Consignar Un (1) Rótulo o Etiqueta del Producto Este modelo deberá contener como mínimo la información de Nombre, Marca, Lote, Fecha de elaboración y Fecha de Vencimiento |
| 6 | Acta de toma de muestra del SENIAT. (para Bebidas alcohólicas nacionales) | Consignar copia |
| 7 | Resultado No Conforme | Copia del resultado analítico con resultado No Conforme. |
| 8 | Muestra Representativa. | Consultar L-DARM-001 Cantidad Mínima de Productos Alimenticios requeridas para el ensayo |
| 9 | Transferencia bancaria con el importe correspondiente al análisis solicitado (ver Regimen tarifario) | Cuenta para transferencia: Banco de Venezuela a la cuenta número N° 0102-0132-2900-0002-3650 RIF G-20000101-1 Consignar una (1) copia |
| 10 | Comprobante de citas | Consignar una (1) copia |
| 11 | Formato identificación del sobre | Imprimir y colocar en el sobre donde entregará toda la documentación |
| (*) EXCEPTO CERTIFICADO DE ANALISIS DE EXPORTACIÓN Coloque esta documentación en un sobre manila debidamente identificado en su parte frontal con el recaudo “Formato de identificación del sobre” Una vez asignada su cita, digitalice los recaudos indicados en formato PDF. (Máximo 300 MB) y envíe vía correo electrónico a la siguiente dirección: divcalimentos@gmail.com | ||
SOLICITUD DE COPIAS SIMPLES Y COPIAS CERTIFICADAS
| N° | Recaudo a consignar | Instrucción |
|---|---|---|
| 1 | Solicite su requerimiento vía correo electrónico a la siguiente dirección: divcalimentos@gmail.com Incluir: Nombre del producto, Marca, Nº de identificación (DAR), Transferencia bancaria | |
| 2 | Transferencia bancaria con el importe correspondiente al trámite solicitado (ver Regimen tarifario) | Cuenta para transferencia: Banco de Venezuela a la cuenta número N° 0102-0132-2900-0002-3650 RIF G-20000101-1 Consignar una (1) Copia |
Para mayor información comuniquese al Número telefónico: 0212-219-16-70 o al correo electronico : divcalimentos@gmail.com
En construcción

En construcción

Bioequivalencia
Los estudios de Biodisponibilidad y Bioequivalencia deben llevarse a cabo en centros o unidades, certificadas por el Instituto Nacional de Higiene “Rafael Rangel”, de acuerdo a lo dispuesto en las Normas Venezolanas de Biodisponibilidad y Bioequivalencia de Productos Farmacéuticos.
- Centros Especializados para Estudios de Biodisponibilidad y Bioequivalencia (CEEB): Que tengan dentro de su infraestructura todas las Unidades Especiales para Estudios de Biodisponibilidad y Bioequivalencia (UEEB). Su certificación tendrá una vigencia de (02) años.
- Unidades Especiales Contratadas para Estudios de Biodisponibilidad y Bioequivalencia (UECEB): Que son convenidas en forma individual por el Patrocinador del estudio. Estas Unidades pueden formar parte a su vez, de un Centro Especializado para Estudios de Biodisponibilidad y Bioequivalencia (CEEB). Su certificación tendrá una vigencia de un (01) año.
La solicitud la autorización de Centros o Unidades para realizar Estudios de Biodisponibilidad y Bioequivalencia, debe realizarse empleando los siguientes Formularios:
- F-PERC-045: Solicitud de Certificación de Centros Especializados para realizar Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-046: Solicitud de Certificación de Unidades Clínicas para realizar Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-047: Solicitud de Certificación de Unidades Bioanalitica donde realizan Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-048: Solicitud de Certificación de Unidades Estadísticas donde realizan Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-049: Solicitud de Certificación de Laboratorios de Análisis Clínicos que prestan servicios a los Centros Especializados o Unidades Clínicas donde se realizan Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-050: Solicitud de Renovación de Centros Especializados donde se realizan Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-051: Solicitud de Renovación de Unidades Clínicas donde realizan Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-052: Solicitud de Renovación de Unidades Bioanalitica donde realizan Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-053: Solicitud de Renovación de Unidades Estadísticas donde realizan Estudios de Biodisponibilidad/Bioequivalencia
- F-PERC-054: Solicitud de Renovación de Laboratorios de Análisis Clínicos que prestan servicios a los Centros Especializados o Unidades Clínicas donde se realizan Estudios de Biodisponibilidad/bioequivalencia.


